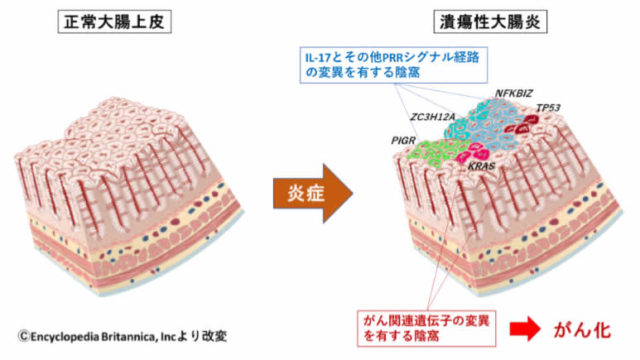
必須微量元素である亜鉛が、どのようにクローン病や潰瘍性大腸炎の病変につながっているかのメカニズムは、ずっと解明されないままでしたが、この年明けに石川県立大学の研究チームらが立証しました。
このことで、今後の炎症性腸疾患の治療の見直しや腸疾患のみならず免疫疾患の治療についても新しい光が見えてきそうです。
IBD患者の亜鉛欠乏データ
今回の研究発表の以前から、IBDとくにクローン病においては患者の亜鉛不足(血中亜鉛濃度)と病変との関係性には注目されてきました。
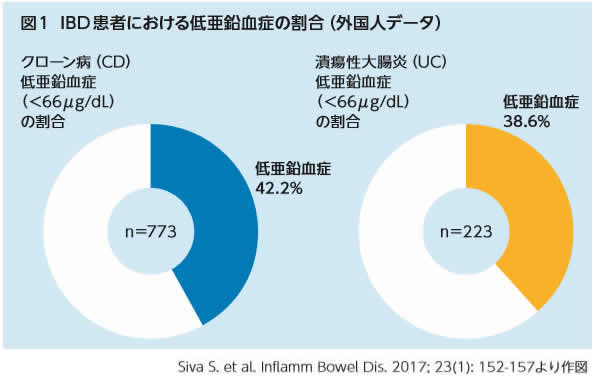
血中の亜鉛の濃度が低い場合、抗ヒトTNF-αモノクローナル抗体製剤、いわゆるレミケードやヒミュラなどの生物学的製剤の効果が薄くなってしまうなどの課題がありました。
亜鉛の不足と免疫疾患の関係性には分かってはいましたが、なかなか踏み込めていなかったという状況です。
近年、亜鉛の吸収メカニズム(亜鉛トランスポーター)の解明について大きな進歩があり期待が高まっていました。
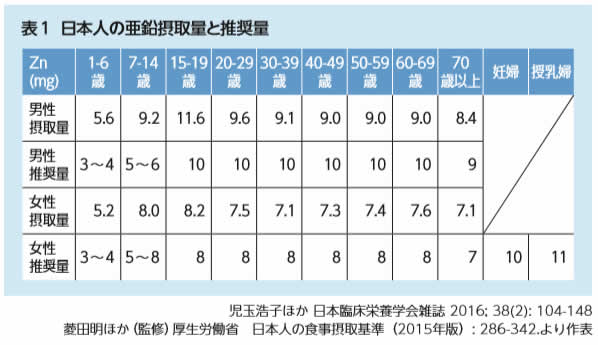
日本の亜鉛摂取量と推奨量
日本人の食事の近代化・欧米化などによる食事習慣の変化により亜鉛の摂取は減少の傾向にあります。
日本人の亜鉛摂取は慢性的に不足していると言えます。
また女性の妊婦・授乳婦は特に亜鉛摂取が低いと言われています。
亜鉛が不足する食事習慣の背景
予想される一因としてはファーストフードや食事制限による必要栄養素の欠如です。
亜鉛は動物性たんぱく質に多く含まれることが多いので、さっぱりした食事が多いと亜鉛不足に陥りがちになります。

亜鉛欠乏による症状
亜鉛が不足することによって代謝能力が落ちるだけでなく、免疫系統の機能不全も起こります。
- 貧血
- 味覚障害
- 皮膚炎・脱毛
- 発育障害(低身長症・成長ホルモンの低下)
- 性腺機能不全(男性の不妊症など)
クローン病あるいは潰瘍性大腸炎の患者さんは亜鉛の欠乏により、イベント発生リスク(入院・手術・合併症)が上がることも分かっています。
今回の研究発表の注目点
現在のクローン病や潰瘍性大腸炎などの炎症性腸疾患の治療は、炎症を起こすメカニズムを解明することよりも、炎症をおこした炎症性サイトカインというたんぱく質をどう抑えるかというアプローチが主流になっていました。
大腸粘膜固有層において炎症型であるM1型Mphの増加ならびに17型ヘルパーT(Th17)細胞が活性化することが判明した。また、Th17細胞の活性化には、M1型Mphから分泌されるインターロイキン-23(IL-23)が関与することを明らかにした。
亜鉛キレーターであるTPENの添加により細胞内亜鉛欠乏を呈したBMDMでは、IL-23を構成するサブユニットであるIL-23p19の発現が有意に亢進することを見出した。さらに、亜鉛欠乏に伴うIL-23p19の発現亢進には、インターフェロン応答型転写因子であるIRF5の核内移行ならびにIL-23p19プロモーター上へのリクルートの促進が関与することを明らかにした。(2020/01/22「QLifePro」より)
今回の研究成果により、「そもそも亜鉛欠乏がなぜ腸の炎症の発生につながるのか?」ということのひとつが解明されたということになります。
こんな研究も「亜鉛による腸粘膜の早期治癒」
同じく、現在の炎症を抑えるアプローチとは違った考え方として、
「炎症が起こったらすぐに回復を促す」という研究もおこなわれています。
火傷に軟膏を塗って治すように、炎症で腸の粘膜上皮が傷ついたところに亜鉛をスピーディに投与することによって、早く再生を促すという考え方です。
実際にこちらは、治験としてステロイドや5-ASAなどの通常治療の上乗せとして亜鉛を投与すると、
治療前に見られた炎症やむくみが、1週間の亜鉛の上乗せ治療で改善したという結果が出ています。
亜鉛を加える薬剤治療を一週間続けることによって炎症細胞が減少し潰瘍性大腸炎の病態改善に効果的であることが示唆されました。
参考「炎症性腸疾患における亜鉛の関与を読み解く」(PDF)